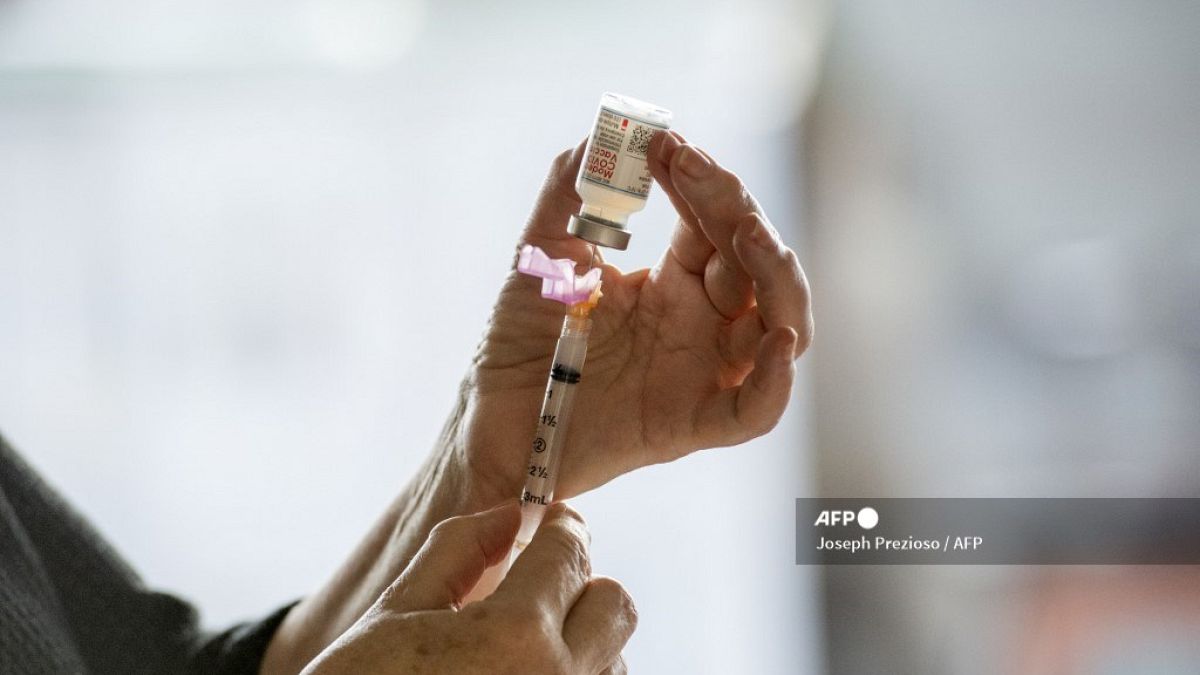
Questionado sobre se a carga administrativa e não o rigor científico é que estão na base da lentidão da EMA, o especialista Stephen Evans diz que tal é inevitável numa decisão tão partilhada.
Com a aprovação, quarta-feira, da vacina contra a Covid-19 da farmacêutica Moderna, a União Europeia passa a dispor de duas das seis vacinas sobre as quais existem contratos de comercialização.
Mas afinal porque é que o processo da Agência Europeia de Medicamentos (AEM) é mais cauteloso e lento do que o de outros reguladores, tais como o do Reino Unido e o dos EUA?
"Existem dois aspetos: a ciência e a administração. A ciência é feita analisando todos os dados de laboratório relativos a estudos com animais, na fase inicial, e depois com humanos, num total de três fases. Esses processos tendem a ser praticamente os mesmos, sejam feitos na Europa, nos EUA ou em qualquer outro lugar. Mas administrativamente podem ser bastante diferentes", explica Stephen Evans, ex-membro independente do Comité de Avaliação de Risco e Segurança de Medicamentos da AEM.
"No contexto da AEM, a avaliação científica é feita principalmente por dois Estados-membros. Por exemplo, para a vacina da Pfizer, foram a Suécia e a França os dois Estados-membros que fizeram a maior parte da avaliação científica. Mas para aprovar a vacina em toda a União Europeia, tem de haver também contribuições de todos os restantes Estados-membros, de especialistas de toda a Europa que participam nas reuniões e dão contribuições para a avaliação científica. Só quando há uma votação favorável de todos os Estados-membros e da Comissão Europeia é que a vacina finalmente é autorizada na Europa", acrescentou.
Questionado sobre se a carga administrativa e não o rigor científico é que estão na base da lentidão da EMA, o especialista diz que tal é inevitável numa decisão tão partilhada.
"Penso que é, provavelmente, justo dizer que não há dúvida de que o processo é rigoroso na AEM. Até recentemente, o Reino Unido teria feito parte desse processo e poderia ter sido o Estado-membro a fazer a avaliação científica. Mas é inevitável que, ao dividir o trabalho entre os 27 Estados-membros, para os envolver a todos nas decisões, tem de haver pelo menos dois Estados-membros que assumem o papel principal de avaliar os dados científicos. Mas a autorização deve ser partilhada por todos os 27 Estados-membros", explicou Stephen Evans.